DE
Gebrauchsanleitung, Reinigung und Pflege - Ophthalmochirurgische Instrumente
1) ZWECKBESTIMMUNG
FIMCO-Instrumente sind ophthalmologische Medizinprodukte zur Durchführung chirurgischer Leistungen wie Schneiden, Einschneiden, Durchstechen, Spreizen, Gespreizthalten, Erhöhen der Gewebesteifigkeit, Ausüben von lokalem Druck, Führen und Biegen eines Implantats, Kalibrieren einer Schleife, Schutz des Auges während der Operation, Zirkulierenlassen einer Flüssigkeit, Reiben, Manövrieren, Handhaben, Kratzen, Ergreifen und Entfernen von Fremdkörpern, Angabe einer Größe, Richtung oder Entfernung, Festklammern, Festklammern zur Prüfung der Dehnbarkeit eines Augenmuskels, Hinterlassen einer Druckstelle, Umfangen einer Flüssigkeit, Abschleifen, Ergreifen von Gewebe, Sondieren und Dilatieren.
FIMCO-Instrumente sind für ophthalmochirurgische Eingriffe vorgesehen. Die Instrumente dürfen in der ophthalmologischen Mikrochirurgie ausschließlich von einer hierfür qualifizierten medizinischen Fachkraft verwendet werden. Die Instrumente werden bei Patienten aller Art (Erwachsene/Kinder/Säuglinge) eingesetzt, die eines chirurgischen Eingriffs bedürfen und bei denen keine Kontraindikation vorliegt.
2) BESCHREIBUNG UND MATERIALIEN
Bei den FIMCO-Instrumenten handelt es sich um wiederverwendbare chirurgische Geräte, die in der Augenchirurgie eingesetzt werden. Alle Instrumente werden in unsterilem Zustand geliefert und müssen vor Gebrauch von der Gesundheitseinrichtung gereinigt und sterilisiert werden.
Die chirurgischen Instrumente bestehen hauptsächlich aus Edelstahl in medizinischer Qualität und können Folgendes enthalten: Titan, Titanlegierung (TA6V), vernickeltes und verchromtes Messing, Silber, Aluminium, Polytetrafluorethylen (PTFE), Polyetheretherketon (PEEK), Silicon, Epoxidharz, Polyoxymethylen (POM-C), Polyphenylsulfon (PPSU), Wolframcarbid, Glas (Pyrex) oder Quarz.
3) INDIKATIONEN
Zum Einsatz gelangen FIMCO-Instrumente in der refraktiven Chirurgie, Kataraktchirurgie, bei Augentrockenheit, in der Glaukomchirurgie, Netzhautchirurgie, Chirurgie der altersbedingten Makuladegeneration (AMD), Dacryocystorhinostomie-Chirurgie, Presbyopie-Chirurgie, Hornhauttransplantations-Chirurgie (Keratoplastik), bei Keratokonus, Chalazion, Hordeolum, Konjunktivitis, Myodesopsie, diabetischer Retinopathie, Keratitis, Optikusneuritis, Pinguecula, Pterygium, Uveitis, in der Strabismus-Chirurgie, zur Enukleation und Exenteration des Auges.
4) KOMBINATION VON MEDIZINPRODUKTEN
Kanülenhalter und -manschetten sowie Luer-Anschlüsse, Silikonanschlüsse und -schläuche und Spritzen von FIMCO dürfen nur mit Kanülen von FIMCO zusammengefügt werden (und umgekehrt). Kombinationen aus FIMCO-Produkten und Erzeugnissen von Wettbewerbern sind mangels Kompatibilitätsprüfung unzulässig. FIMCO übernimmt keine Verantwortung für Unfälle, die sich aus einer Zusammenfügung von dessen Medizinprodukten mit solchen von Wettbewerbern ergeben.
Bei Bedarf können die Silikonschläuche der Doppelstromkanülen ersetzt werden. Die Doppelstromkanüle F528C muss mit dem Silikonschlauch Ø1,5 mm verwendet werden. Für alle anderen Doppelstromkanülen ist ein Silikonschlauch Ø1,1 mm zu verwenden.
5) LEISTUNGSMERKMALE DER PRODUKTE UND ERWARTETER KLINISCHER NUTZEN
Die Leistung der Instrumente bemisst sich nach deren korrekter Nutzung entsprechend der diesen zugedachten Verwendung mit der geeigneten chirurgischen Technik und nach der Leistung der zugehörigen Geräte. Auf Grundlage der klinischen Bewertung und des aktuellen Kenntnisstands/des Stands der Technik werden alle Restrisiken bei Abwägung gegen den Nutzen für den Patienten als akzeptabel eingestuft.
6) GEGENANZEIGEN
- Allergie oder Empfindlichkeit gegenüber in den Instrumenten verwendeten Materialien
- Jede gesundheitliche Beeinträchtigung, der einem reibungslosen Ablauf des chirurgischen Eingriffs entgegenstünde
- Jeder Fall, der nicht in den Indikationen beschrieben ist
7) POTENTIELS EFFETS INDÉSIRABLES, COMPLICATIONS ET RISQUES RÉSIDUELS
Die nachfolgend aufgeführten Restrisiken, Nebenwirkungen und Komplikationen, die beim Einsatz der FIMCO-Instrumente möglicherweise auftreten, können einen erneuten Eingriff erforderlich machen oder eine Verlängerung der Eingriffsdauer zur Folge haben:- Verletzung des Patienten oder der Bedienperson
- Zerbrechen des Instruments / Gefahr, dass Trümmerteile in den Patienten gelangen. Beschädigte oder zerbrochene Instrumente können für den Nutzer, den Patienten oder Dritte gefährlich sein
- Gefäß- oder Gewebsverletzung
- Postoperative Infektion
- Entzündliche Reaktion
- Zerlegen von Komponenten
- Vorzeitiger Verschleiß / Beschädigung der Instrumente durch unsachgemäße Verwendung
8) HANDHABUNG DER INSTRUMENTE
Die Gesundheitseinrichtung ist dafür verantwortlich, dass die Instrumente vor deren Einsatz nach validierten Verfahren vorgereinigt, gereinigt und sterilisiert werden. Die folgenden Empfehlungen ersetzen ausdrücklich nicht die geltenden Gesundheitsvorschriften in Gestalt von Normen, Leitfäden, Regierungsanweisungen, ministeriellen Texten usw. Reinigungsverfahren, die ohne Einhaltung der Validierungsbereiche praktiziert werden, können Toxizitätsrisiken bergen oder den sterilen Zustand des Instruments gefährden.
In funktioneller Hinsicht ist vor dem Einsatz eine Inspektion durchzuführen, um sicherzustellen, dass keine Grate oder Rückstände vorhanden sind, die das Gewebe des Patienten oder auch die Schutzausrüstung des Personals beschädigen könnten. Bei der Inspektion ist auf Anzeichen von Korrosion oder Kontamination zu achten, da diese zu Infektionen, Entzündungsreaktionen oder Instrumentenbrüchen führen könnten. Außerdem ist die Unversehrtheit der Instrumente zu kontrollieren (abnormale Größe oder Griffigkeit, beschädigte oder abgenutzte Oberfläche, abgesplittertes Material, Lesbarkeit der Markierung und der Maße sowie Spiel, Zustand der Klingen von Messern und Scheren). Schließlich noch ist die Funktionsfähigkeit (Öffnen, Schließen, Arretieren) der Vorrichtungen vor dem Eingriff mehrfach zu kontrollieren: Diese dürfen keinen zu großen Widerstand aufweisen. Jedes Gerät, das in irgendeiner Weise für defekt oder nicht funktionsfähig befunden wird, ist zur Wartung oder zum Austausch an FIMCO zurückzusenden. Die folgenden Anweisungen sind stets zu befolgen, um die optimale Wirksamkeit und Sicherheit der Instrumente zu bewahren:- Chlor-, aldehyd-, alkohol- und säurehaltige Reinigungsmittel und Chemikalien dürfen ebenso wenig verwendet werden wie Scheuermittel, welche die Instrumente beschädigen könnten.
- Zur Neutralisierung von alkalischen Rückständen nach dem automatisierten maschinellen Reinigungszyklus in und an Instrumentenkästen und Instrumenten, die aus Polymerteilen bestehen (Beispiel: Griffe), darf keine Phosphorsäure verwendet werden.
- Die Temperatur der Vor-Desinfektion sollte < 45 °C betragen, um das Risiko eines Festbackens von Rückständen zu vermeiden.
Die Anwendungshinweise sind ebenso wie alle Angaben zu Temperatur, Konzentration, Einwirkzeit usw. genauestens zu beachten. Andernfalls können Probleme mit den Instrumenten auftreten, z. B. visuelle Veränderungen an den Materialien (Verfärbungen).
Instrumente, auf denen sich eine Oxidschicht gebildet hat, können andere Instrumente verunreinigen; dementsprechend dürfen oxidierte Instrumente nicht mit intakten Instrumenten gemischt werden, damit Kontakte vermieden werden, welche den sterilen Zustand gefährden könnten.
Alle Mitarbeiterinnen und Mitarbeiter, die mit verunreinigten Instrumenten in Berührung kommen, sind gehalten, auf gute Hygiene zu achten und geeignete Schutzausrüstung (Handschuhe, Maske, Schürze usw.) zu verwenden.
Scharfe oder spitze Geräte sind mit äußerster Vorsicht zu handhaben.
a. Schmieren und Fetten
Nach Gebrauch und Reinigung ist es hin und wieder erforderlich, die Gelenkteile bzw. jegliche beweglichen Teile der Instrumente zu schmieren. Hierzu ausschließlich sterilisierbares, wasserdampfdurchlässiges Wartungsöl in Form von Weißöl ohne Zusatzstoffe verwenden, das eine zertifizierte Biokompatibilität aufweist und für die Sterilisierung (feuchte Hitze) zugelassen ist. Die der Größe des Instruments entsprechende Öldosis unmittelbar auf den Gelenkbereich auftragen. Das Öl durch wiederholtes Öffnen und Schließen des Instruments gleichmäßig verteilen. Überschüssiges Öl mit einem sauberen, nicht fusselden Tuch entfernen.
b. Kontrolle, Wartung und Überprüfung
Nach jedem Gebrauch und jeder Reinigung:- Das Instrument nach erfolgter Reinigung auf Raumtemperatur abkühlen lassen.
- Das Instrument auf Sauberkeit, Funktionalität und Schäden kontrollieren und Instrumente aussondern, die verbogen, verformt, abgenutzt, geknickt, gebrochen oder rissig sind; ebenso solche Instrumente, deren Teile demontiert worden sind.
- Die Kompatibilität zwischen einander zugehörigen Instrumenten überprüfen.
- Ein beschädigtes Instrument sofort entfernen.
c. Verpackung
- Instrumente mit dünnen Spitzen geschützt aufbewahren.
- Instrument in das dafür vorgesehene Aufbewahrungsfach oder auf das entsprechende Tablett legen. Dabei darauf achten, dass scharfe Klingen geschützt sind.
- Die Tabletts entsprechend dem Sterilisationsverfahren verpacken (dabei darauf achten, dass die Verpackung eine neuerliche Kontamination des Instruments zwischen der Abschlussphase seiner Aufbereitung und seiner nächsten Verwendung verhindert).
- Die Instrumente in geeigneten Sterilisationsverpackungen verpacken, die es ermöglichen, den sterilen Zustand bis zur nächsten Verwendung zu bewahren.
- Bei längeren Zeiträumen sind die Mikrozangen (F250A, F250A5, F251A, F251A5, F251A9, F251B, F251B5, F253A, F253A5, F253A9, F253B, F254A, F255A, F143MI und F144MI) am Ende der Vorreinigung zu schmieren (vgl. Teil 9).
9) VORREINIGUNGSBEHANDLUNG
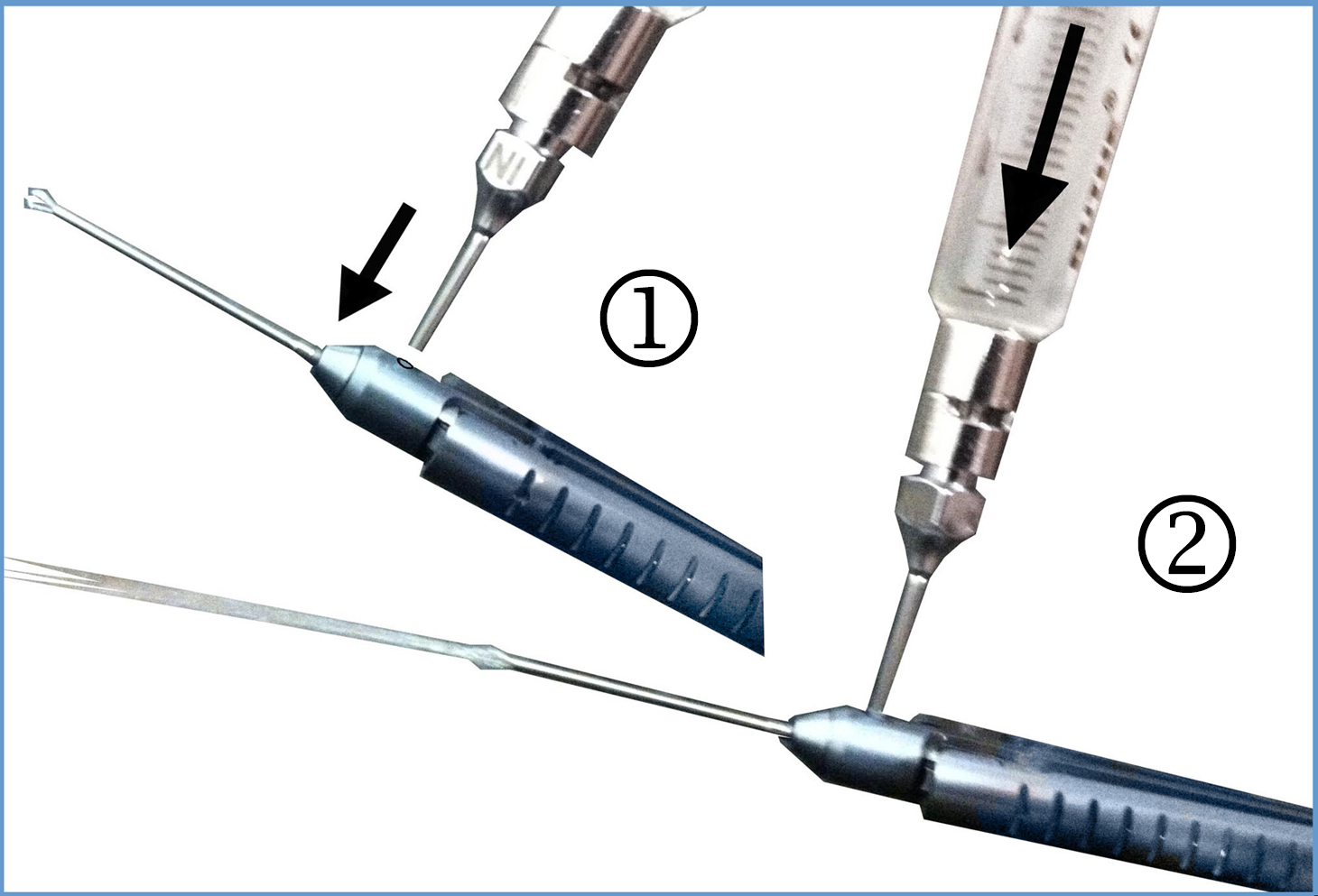
Die Mikrozangen (F250A, F250A5, F251A, F251A5, F251A9, F251B, F251B5, F253A, F253A5, F253A9, F253B, F254A, F255A, F143MI und F144MI) sind vor der automatischen Reinigung über die mit dem Instrument gelieferte Kanüle mit dem Reinigungsmittel der Gesundheitseinrichtung zu reinigen:- Schritt 1: Die Kanüle in die Öffnung einführen
- Schritt 2: Das Reinigungsmittel injizieren
- Schritt 3: Die Schritte 1 und 2 mit kontrolliertem Wasser wiederholen
Eingetrocknete Rückstände können den Reinigungsprozess erschweren und unwirksam machen oder die Korrosion von rostfreiem Stahl beschleunigen. Das Verfahren der Vor-Desinfektion zielt darauf ab, die anschließende Reinigung zu vereinfachen. Außerdem soll es das Personal bei der Handhabung der Instrumente schützen und einer Kontamination der Umwelt entgegenwirken.
Alle wiederverwendbaren Produkte sind nach Gebrauch unverzüglich einer Vor-Desinfektionsbehandlung zu unterziehen oder in einem Reinigungs- und Desinfektionsgerät aufzubereiten. Sollte eine sofortige Vor-Desinfektion nicht möglich sein, können die Instrumente bis zu dieser in entmineralisiertem Wasser aufbewahrt werden.
- Die Vor-Desinfektionsbehandlung erfolgt durch Eintauchen der Instrumente über mindestens 15 Minuten in eine neutrale oder alkalische Lösung, die weder einen Aldehyd noch Ethanol enthält. Vorzugsweise eine Lösung verwenden, welche Proteine nicht bindet. Die Gebrauchsanweisungen strikt befolgen und sich zuvor vergewissern, dass die Produkte mit den Instrumenten kompatibel sind.
- Geeignete Reinigungs- und Desinfektionsmittel verwenden. Sollte es zwischen der Vordesinfektion und der Reinigung zu einer Verzögerung kommen, ist das Instrument gründlich unter fließendem Wasser zu spülen, ehe Sie es mit einem Reinigungs- und Desinfektionsgerät reinigen und desinfizieren.
- Die Instrumente erforderlichenfalls mit Ultraschall reinigen, vgl. Abschnitt Reinigung.
- Alle erkennbaren organischen Rückstände (Blut, Knochenmaterial usw.) beseitigen; besondere Aufmerksamkeit ist bei hohlen oder gerillten Vorrichtungen geboten.
- Die Verwendung von Drahtbürsten, Scheuerschwämmen oder anderen Gegenständen, die die Instrumente beschädigen könnten, ist zu vermeiden. Zur Reinigung der Teile von jeglichen biologischen Rückständen (Blut, Knochenmaterial usw.) , die potentiell die Wirkung von Reinigungs- und Dekontaminationsmitteln beeinträchtigen, ist die Verwendung von Bürsten mit weichen Borsten und Tupfern vorzuziehen, deren Größe an die zu behandelnden Geräte angepasst ist. Besondere Aufmerksamkeit ist bei kanülierten Vorrichtungen geboten
- Es empfiehlt sich die Verwendung einer mechanischen Einwirkung durch Hand- oder Ultraschallgeräte (Abschnitt 10a).
- Instrumente, die sich zerlegen lassen, sollten vor dem Vordesinfektionsverfahren zerlegt werden (außer bei Zweistromkanülen, die die ganze Zeit zusammengefügt bleiben sollten). Darüber hinaus sollten die Gelenke von Vorrichtungen, deren bewegliche Komponenten die Demontage erschweren, in der Vor-Desinfektionsbehandlungsstufe manuell bewegt werden, um zusätzliche Rückstände zu entfernen.
- Die Instrumente vorzugsweise in eine Lösung aus einem enzymhaltigen Reiniger und einem damit kombinierten Desinfektionsmittel eintauchen, das Proteine nicht bindet. Von einer Verwendung von aldehydhaltigen Desinfektionsmitteln, die eine bindende Wirkung haben, ist abzusehen. Die vom Hersteller empfohlenen Anwendungsbedingungen beachten und sich vergewissern, dass das Produkt mit den Instrumenten kompatibel ist.
- Die Instrumente anschließend gründlich mit kontrolliertem Wasser abspülen, um Interferenzen zwischen Reinigungslösungen zu vermeiden. Die Anweisungen des Herstellers dieser Produkte sind unbedingt zu beachten.
- Lange Wartezeiten bei die Behandlung – beispielsweise über Nacht oder das Wochenende – sind wegen des Korrosionsrisikos und der Gefahr einer Beeinträchtigung der Wirksamkeit der Reinigung zu vermeiden. Das Eintauchen in entmineralisiertes Wasser verhindert ein Antrocknen von Rückständen und vereinfacht die anschließende Reinigung.
- Bei langen Zeiträumen zwischen Vordesinfektion und Reinigung sind die Instrumente vor der Reinigung und Desinfektion in einem Reinigungs- und Desinfektionsgerät in kontrolliertem Wasser zu waschen.
- die Dampfsterilisation bei 134 °C über 18 Minuten,
- das Eintauchen in 1-molare Natriumhydroxid-Lösung über 1 Stunde bei Raumtemperatur,
- das Eintauchen in 2-prozentige Natriumhypochlorit-Lösung über 1 Stunde bei Raumtemperatur.
- Für eine Maximierung der Lebensdauer und der Effizienz der Instrumente sind Pflege und Wartung unverzichtbar.
- Die Instrumente nicht biegen und keinen großen Kräften aussetzen, da dies zum Bruch oder Versagen mit der möglichen Folge von Verletzungen des Patienten oder der Bedienperson führen könnte.
- Nicht versuchen, das Instrument zu verändern.
- Der Nutzer hat sich vor der Verwendung der Ausrüstung zu vergewissern, dass diese sich in gutem Zustand befindet, ordnungsgemäß funktioniert und insbesondere keine Spuren von Korrosion aufweist.
- Jedes Instrument vor der Verwendung einer Sichtprüfung auf Abnutzung, Verformung, Verdrehung, Beschädigung, Kontamination und Defekte unterziehen und gegebenenfalls aussondern. Für unbrauchbar befundene Instrumente unmittelbar durch neue ersetzen (mit Ausnahme von kontaminierten Instrumenten, die vor Gebrauch gereinigt, desinfiziert und sterilisiert werden müssen).
- Alle Instrumente unterliegen bei häufiger Verwendung einem natürlichen Verschleiß. Die am häufigsten verwendeten und empfindlichsten Instrumente regelmäßig ersetzen, insbesondere dann, wenn diese dazu neigen, sich zu verbiegen, zu verformen oder abzunutzen (insbesondere Sonden und Manipulatoren).
- Geht ein Instrument bei einem Eingriff zu Bruch, sind alle Bruchfragmente und Trümmer aus dem Patienten zu entfernen.
- Darauf achten, dass auf dem Bereich der Lasermarkierung keine Feuchtigkeit zurückbleibt. Wenn sich ein bräunlicher Fleck bildet, diesen mit einem weichen Tuch mit Druck abwischen.
- Beim Einsatz können auf die Geräte Kräfte verschiedener Art einwirken, die sich nicht immer vorhersehen lassen. Selbst bei ordnungsgemäßer Wiederaufbereitung, Wartung und Inspektion können die Geräte während eines Eingriffs das Ende ihrer Lebensdauer erreichen. Dem Chirurgen muss daher ein Ersatz oder eine Alternative zur Verfügung stehen.
- FIMCO-Instrumente dürfen nur für die Funktionen verwendet werden, für die sie vorgesehen sind.
- Beim Artikel F807C (Roth-Rapp-Myometer) ist es zwingend erforderlich, jede Zugbewegung in der Achse des Instruments (Längsachse) durchzuführen. Andernfalls wird ein fehlerhafter Wert für die Muskeldehnung ermittelt.
- Galezowski-Sonden (F600A, F601A, F602A, F603A, F604A, F605A, F606A, F607A, F608A, F609A, F610A, F610B) und doppelte Bowman-Sonden (F610C, F611A, F612A, F613A, F614A und F614B) müssen von der Einführung bis zum Herausziehen so weit wie möglich an der Achse des Tränenkanals ausgerichtet sein. Andernfalls besteht die Gefahr, dass die Geräte zerbrechen und den Patienten verletzen.
ACHTUNG: Tabletts und Körbe dürfen nicht über einen längeren Zeitraum mit Dekontaminationslösungen in Berührung kommen. Vernickelte/verchromte Kanülen und Aluminiumdosen dürfen niemals mit Natriumhydroxid in Berührung kommen, da sie andernfalls korrodieren. Verschmutzte Bereiche sofort reinigen und abspülen.
10) REINIGUNG
Die Instrumente sind, soweit das Zusammenfügen/Zerlegen möglich ist, nach dem Zerlegen gründlich zu reinigen. Es empfiehlt sich die ausschließliche Verwendung von mechanisierten Methoden zur Vor-Desinfektion und Reinigung mit einem Reinigungs- und Desinfektionsgerät, das den Anforderungen der Normenreihe ISO 15883 entspricht. Die Anweisungen des Herstellers für die Verwendung des Reinigungs- und Desinfektionsgeräts beachten. Das Reinigungsmittel muss mit den medizinischen Anwendungen und den Instrumentenmaterialien kompatibel sein und darf keine bekannte Resttoxizität für den Patienten aufweisen. Lässt sich der Prozess nicht automatisch durchführen, so ist ein manueller Prozess zu verwenden, bei dem die in den Reinigungsempfehlungen beschriebenen Bedingungen nachgestellt werden. Der Reinigungszyklus muss eine abschließende Spülung mit kontrolliertem Wasser beinhalten. Die Dauer, der Wasserdurchsatz und die Spülmengen sind so zu bemessen, dass die Reinigungsmittelrückstände auf der Produktoberfläche auf das geringst mögliche Maß reduziert werden. Zur Vermeidung jeglicher Rekontamination sind die Instrumente anschließend gründlich zu trocknen.
a. Reinigung mit Ultraschall
Diese Reinigungsmethode eignet sich besonders für Instrumente mit Gewinde oder tiefen Rillen. Die Ausrüstung ist vom Nutzer zu validieren und darf ausschließlich mit Produkten eingesetzt werden, die für die Instrumentenmaterialien geeignet sind. Zur Vorreinigung der Instrumente von eingetrockneten Rückständen oder als wirksame mechanische Unterstützung vor der Reinigung und Desinfektion in einem Reinigungs- und Desinfektionsgerät eine 10- bis 20-minütige Ultraschallreinigung durchführen.
b. Automatische Reinigung
Kontrollieren, dass das Reinigungs- und Desinfektionsgerät zugelassen ist (CE-Kennzeichnung), sich in einem einwandfreien Wartungszustand befindet und den geltenden Normen entspricht. Ausschließlich Produkte verwenden, die mit den Instrumenten kompatibel sind, keinen Aldehyd enthalten und ggf. das Prion Standard Protocol (PSP) erfüllen. Die Anleitungen hinsichtlich Konzentration, Temperatur und Einwirkzeit beachten.
Reinigungsmittel mit neutralem oder alkalischem pH-Wert verwenden. Die Waschverfahren befolgen, um einen angemessenen Schutz der Instrumente zu gewährleisten. Im Anschluss an die Reinigung und Desinfektion im Reinigungs- und Desinfektionsgerät kontrollieren, ob alle Rückstände entfernt worden sind. Erforderlichenfalls den Reinigungsvorgang durch Bürsten wiederholen, bis alle sichtbaren Rückstände beseitigt sind.
Tabelle 1 – Empfohlenes Protokoll für die automatische Reinigung
| Abschnitt | Dauer | Empfohlene Temperatur | Art des Wassers/des Reinigungsmittels |
|---|---|---|---|
| Vorreinigung | 4 min | kalt (<30°C) | Wasser |
| Reinigung | 10 min | erwärmt, 55°C | Neodisher Septoclean* 10mL/L(1%) |
| Zwischenspülung | 3 min | >30°C und <60°C | Enthärtetes oder entmineralisiertes Warmwasser |
| Thermische Desinfektion | 5 min | erwärmt, 90°C | Demineralisiertes heißes Wasser |
| Trocknung | 20 min | Luft bei 99°C | unzutreffend (Luft) |
*oder uneingeschränkt gleichwertiges Produkt
Ggf. die Restfeuchtigkeit mit einem zusätzlichen Trocknungszyklus in der Maschine oder mit fusselfreien Rechtecktüchern und Druckluft ohne kondensationsbedingte Wasserpartikel beseitigen.
Hinweis: Bei Patienten, bei denen der Verdacht auf oder die Erkrankung an transmissibler spongiformer Enzephalopathie (TSE) besteht, ist das Reinigungsverfahren im Reinigungs- und Desinfektionsgerät nach einem Dekontaminationsverfahren entsprechend der Anweisung DGS/RI3/2011/449 durchzuführen.
Es gibt drei Verfahren, von denen indes keines eine absolute Garantie bietet:Vor einer Verwendung von Natriumhypochlorit oder Natriumhydroxid ist abzuraten, da die Instrumente hierdurch korrodieren würden. Keine der drei Methoden bietet absolute Gewähr. Gemäß dem Leitfaden der Weltgesundheitsorganisation (WHO) besteht die sicherste, keine Zweifel lassende Methode zur Vermeidung einer Restinfektiosität von kontaminierten Instrumenten und anderen Materialien darin, diese zu entsorgen und durch Verbrennen zu vernichten.
11) STERILISIERUNG
Die Instrumente sind vor der Verwendung zu sterilisieren. Sie müssen mit einer Wasserdampfsterilisation einer Temperatur von maximal 140 °C kompatibel sein. In Übereinstimmung mit den behördlichen Anweisungen zur Vermeidung einer Übertragung von nicht-konventionellen übertragbaren Erregern und mit den geltenden Normen (einschließlich ISO 17665-1) empfiehlt sich die Verwendung einer Dampfsterilisation (gemäß den Anforderungen der Normenreihe ISO 17665) mit einem validierten Zyklus, der eine 18-minütige Behandlung bei 134 °C/2 bar und einen anschließenden Vakuumtrocknungszyklus von mindestens 30-minütiger Dauer umfasst. Die verwendete Verpackung muss für die Verwendung als Sterilbarriere für die Sterilisation im Autoklaven das CE-Zeichen tragen. Vor dem Gebrauch Küchenpapier zum Verpacken verwenden. Der Sterilisations- und Trocknungszyklus ist vom Endanwender entsprechend den Empfehlungen des Herstellers des Sterilisators zu validieren.
Die Instrumente sind in einem geeigneten Beutel zu verpacken, der es ermöglicht, den sterilen Zustands zu bewahren. Auf dem Beutel ist das Sterilisationsdatum und das Ablaufdatum entsprechend den Angaben des Beutelherstellers zu vermerk.
Alle anderen Sterilisationsverfahren (mit Ethylenoxid oder Wasserstoffperoxid bei niedriger Temperatur) werden nicht empfohlen und liegen in der alleinigen Verantwortung des Benutzers.
Die Instrumente sind so vorzubereiten, dass alle Oberflächen dem Wasserdampf unmittelbar ausgesetzt sind: Instrumente mit Scharnier und Schiebe-Instrumente müssen leicht geöffnet sein. Instrumente mit Schutzabdeckungen, die mit "STERILISABLE" gekennzeichnet sind, müssen mit diesen zusammen sterilisiert werden. Komplexe Instrumente, die sich von Hand zerlegen lassen, sind zu zerlegen, und alle Teile sind in der Sterilisationsbox zu verkeilen. Gesundheitseinrichtungen sind gehalten, ihre Ausrüstung und Verfahren, die sie für die Sterilisation in Autoklaven verwenden, durch feuchte Hitze mit geeigneten Techniken zu validieren und zu qualifizieren, und dies in Übereinstimmung mit den geltenden Normen für die Sterilisation von Medizinprodukten. Die Gesundheitseinrichtung trägt die Letztverantwortung für den wirksamen Vollzug der Sterilisation der Produkte und dafür, dass diese in sterilem Zustand verbleiben.
Die Sterilisationsempfehlungen dienen nur zur Orientierung. Der Nutzer/Betreiber ist zur Einhaltung der gesetzlichen und verordnungsrechtlichen Bestimmungen des Landes, in dem er ansässig ist, verpflichtet. Unter keinen Umständen kann der Hersteller für eine mangelnde Sterilität von Produkten, die in der Gesundheitseinrichtung sterilisiert worden sind, haftbar gemacht werden.
12) WIEDERVERWENDUNG VON INSTRUMENTEN
Die Instrumente sind zur Wiederverwendung bestimmt. Die Anzahl der Wiederverwendungen hängt von der Integrität des jeweiligen Instruments ab. Die Wiederverwendung unterliegt keinen theoretischen Beschränkungen und bleibt daher möglich, solange die geforderte Leistung erbracht wird und das Instrument keine Anzeichen von Verschleiß, Verbiegung, Beschädigung oder Leistungsverlust aufweist.
Vor einer Wiederverwendung sind die Geräte (wie in den vorstehenden Abschnitten beschrieben) vorzudesinfizieren, zu reinigen und zu sterilisieren.
13) LAGERUNG, HANDHABUNG UND TRANSPORT
Chirurgische Instrumente sorgsam behandeln und in einem sauberen Raum unter normalen Feuchtigkeitsbedingungen lagern. Die Instrumente vor UV-Strahlung und korrosiven Umgebungen schützen. Müssen sterilisierte Instrumente zum Einsatzort (OP) transportiert werden, so ist dabei deren Sterilität zu bewahren. Zur Erhaltung des sterilen Zustands der Instrumente eine sterile Verpackung verwenden. In Hinblick auf die Gefahr von Stürzen und/oder Verletzungen stets wachsam bleiben.
Zur Vermeidung unnötiger Kontamination gebrauchte Instrumente in einer geschlossenen oder abgedeckten Verpackung zur Beschaffungsstelle transportieren.
Ein Sturz kann den Bruch oder eine Beschädigung des Instruments und/oder Verletzungen der Bedienperson zur Folge haben. Tabletts oder feste Behälter verwenden.
14) ENTSORGUNG UND NICHT FUNKTIONIERENDE INSTRUMENTE
Das Ende der Lebensdauer eines jeden Produkts ist dann erreicht, wenn dessen Merkmale oder Leistung darauf hindeuten, dass die Gesundheit oder die Sicherheit des Patienten oder des Anwenders gefährdet sein könnten. Die Lebensdauer des Geräts hängt von vielen Faktoren ab, einschließlich, ohne sich hierauf zu beschränken, der Art und Weise sowie der Dauer der Verwendung und des Maßes an Wiederaufbereitungen. FIMCO gibt daher keine Höchstzahl an Nutzungen vor. Eine gründliche Inspektion und Funktionstests sind stets durchzuführen.
Schneidkanten, Tüllen, Spitzen, Stifte, Schäfte und Merkmale des Arbeitsendes je nach Lage des Falls auf stumpfe Kanten, Absplitterungen, Verformungen, Risse oder andere Anzeichen für Alterung oder eine Gefährdung der strukturellen Integrität untersuchen. Die Lasermarkierung muss lesbar bleiben. Sobald das Gerät eines dieser Abnutzungszeichen oder andere Hinweise auf eine Fehlfunktion aufweist, empfiehlt es sich, den Gebrauch einzustellen und das Gerät zu ersetzen. Bewegliche Teile betätigen und die Vorrichtungen zur Überprüfung zusammenbauen, dass diese nicht verklemmt oder verstopft sind. Weisen bewegliche oder zusammengebaute Teile eine eingeschränkte Funktionalität auf, so sind die entsprechenden Vorrichtungen zu ersetzen.
FIMCO bietet für seine Instrumente Reparatur-(Wiederaufarbeitungs-)leistungen an und kann den Zustand eines Instruments bewerten. Alle nicht funktionsfähigen oder reparaturbedürftigen Geräte sind in sterilem Zustand und mit einem Sterilisationsnachweis an FIMCO zurückzusenden, da FIMCO für die sichere Entsorgung seiner Geräte sorgt. Wird ein nicht funktionsfähiges Instrument ohne Nachweis der Sterilisation eingesandt, wird das Instrument an die Gesundheitseinrichtung zurückgesendet.
15) GEFAHREN UND VORSICHTSMASSNAHMEN
Der Hersteller empfiehlt, alle Mitarbeiterinnen und Mitarbeiter, die für die Handhabung und Verwendung der Geräte verantwortlich sind, mit den vorliegenden Informationen vollumfänglich vertraut zu machen. Die Verwendung des chirurgischen Instrumentariums setzt Kenntnisse in Anatomie, Biomechanik und Augenchirurgie voraus.
Hinweis: Die in der vorliegenden Gebrauchsanleitung enthaltenen Anweisungen wurden von FIMCO für die Vorbereitung von wiederverwendbaren chirurgischen Instrumenten von FIMCO in Hinblick auf deren Wiederverwendung freigegeben. Es obliegt dem Nutzer/Verantwortlichen, sicherzustellen, dass die Behandlung, wie sie unter Einsatz der Ausrüstung, des Materials und des Pflegepersonals tatsächlich durchgeführt wird, das gewünschte Ergebnis erzielt. Dies erfordert eine routinemäßige Überprüfung und/oder Validierung und Kontrolle der Abläufe.
Es obliegt dem Chirurgen, dem Patienten vor dem Eingriff alle erforderlichen Informationen zukommen zu lassen, einschließlich der Nebenwirkungen, die mit der Operation, den Implantaten und den Instrumenten verbunden sind.
FIMCO übernimmt keine Haftung für Vorfälle, die auf Eingriffe am Instrument durch eine hierzu nicht befugte Person zurückzuführen sind. Die Garantie erlischt, wenn das Instrument außerhalb von FIMCO zerlegt, verändert oder daran gearbeitet wird.
FIMCO weist jegliche Haftung für unmittelbare und mittelbare Nachteile von sich, die dem Kunden durch eine unsachgemäße Verwendung, Wartung, Reinigung oder Sterilisierung des Medizinprodukts entstehen.
16) SCHWERWIEGENDER VORFALL
Als „schwerwiegender Vorfall“ gilt jeder Vorfall, der direkt oder indirekt zu einer der folgenden Situationen geführt hat, geführt haben könnte oder führen könnte: Tod eines Patienten, Nutzers oder einer anderen Person; vorübergehende oder dauerhafte schwerwiegende Verschlechterung des Gesundheitszustands eines Patienten, Nutzers oder einer anderen Person; schwerwiegende Bedrohung der öffentlichen Gesundheit.
Jeder schwerwiegende Vorfall, der sich im Zusammenhang mit FIMCO-Instrumenten ereignet hat, ist FIMCO und der zuständigen Behörde des Mitgliedstaates, in dem der Anwender und/oder Patient niedergelassen ist, zu melden.

Fassung i - 20/06/2022
