FR
Notice d’utilisation, nettoyage et entretien - Instruments de chirurgie ophtalmologique
1) UTILISATION PRÉVUE
Les instruments FIMCO sont des dispositifs médicaux ophtalmologiques destinés à accomplir des actes chirurgicaux tels que couper, inciser, percer, écarter, maintenir écarté, augmenter la rigidité des tissus, appliquer une pression localisée, guider et plier un implant, calibrer une boucle, protéger l’oeil pendant l’opération, laisser circuler un fluide, frotter, manoeuvrer, manipuler, gratter, saisir et retirer des corps étrangers, indiquer une dimension, une orientation ou une distance, accrocher, accrocher et tester l’allongement du muscle, laisser une marque grâce à une pression, contenir un liquide, ronger, saisir un tissu, sonder et dilater.
Les instruments FIMCO sont destinés à des opérations chirurgicales ophtalmologiques. Les instruments doivent être utilisés en microchirurgie ophtalmologique par un professionnel de santé qualifié. Les instruments sont utilisés sur tout type de patients (adultes – enfants – bébés) qui requièrent de la chirurgie et n’ont pas de contre-indication.
2) DESCRIPTION ET MATÉRIAUX
Les instruments FIMCO sont des dispositifs chirurgicaux réutilisables utilisés en chirurgie ophtalmologique. Tous les instruments sont livrés à l’état non-stérile et doivent être nettoyés et stérilisés par l’établissement de santé avant utilisation. Les instruments chirurgicaux sont principalement constitués d’acier inoxydable de qualité médicale et peuvent inclure : titane, alliage de titane (TA6V), laiton nickelé-chromé, argent, aluminium, polytétrafluoroéthylène (PTFE), polyéther éther cétone (PEEK), silicone, résine époxyde, polyoxyméthylène (POM-C), polyphenylsulfone (PPSU), carbure de tungstène, verre (Pyrex), ou quartz.
3) INDICATIONS
Les instruments FIMCO sont utilisés en chirurgie réfractive, chirurgie de la cataracte, sécheresse oculaire, chirurgie du glaucome, chirurgie de la rétine, chirurgie de la dégénérescence maculaire liée à l’âge (DMLA), chirurgie de la dacryocystorhinostomie, chirurgie de la presbytie, chirurgie de greffe de cornée (kératoplastie), kératocône, chalazion, orgelet, conjonctivite, myodésopsie, rétinopathie diabétique, kératite, névrite optique, pinguecula, pterygion, uvéite, chirurgie du strabisme, énucléation oculaire et éviscération.
4) COMBINAISON DE DISPOSITIFS MÉDICAUX
Les manches et manchettes porte-canules ainsi que les raccords Luer, les raccords et tubes silicone et les seringues de FIMCO doivent être assemblés uniquement avec les canules de FIMCO (et réciproquement). Il est interdit de réaliser des montages entre des dispositifs de FIMCO et des dispositifs de la concurrence : la compatibilité n’a en effet pas été vérifiée. FIMCO décline toute responsabilité en cas d’accident issu de montage entre ses dispositifs et ceux de la concurrence.
Si besoin, les tubes silicone des canules double-courant peuvent être remplacés. La canule double-courant F528C doit être employée avec le tube silicone Ø1.5 mm. Toutes les autres canules à double-courant doivent être utilisées avec le tube silicone Ø1.1mm.
5) CARACTERISTIQUES DE PERFORMANCE DES DISPOSITIFS ET BÉNÉFICES CLINIQUES ATTENDUS
La performance des instruments est la réalisation correcte de leur utilisation prévue en fonction de la technique chirurgicale et de la performance des dispositifs associés. Sur la base de l’évaluation clinique, tous les risques résiduels sont jugés acceptables lorsqu’ils sont mis en balance avec les avantages pour le patient, sur la base des connaissances actuelles/de l’état de l’art.
6) CONTRE-INDICATIONS
- Allergie ou sensibilité aux matériaux des instruments
- Toute condition qui empêcherait le bon déroulement de l’intervention chirurgicale
- Tout cas non décrit dans les indications
7) POTENTIELS EFFETS INDÉSIRABLES, COMPLICATIONS ET RISQUES RÉSIDUELS
Les risques résiduels, effets indésirables et complications qui peuvent se produire avec l’utilisation des instruments FIMCO qui sont listés ci-dessous peuvent amener à une nouvelle opération ou à une augmentation du temps opératoire :- Blessure patient ou opérateur
- Casse de l’instrument / risque de débris dans le patient. Des instruments abîmés ou cassés peuvent être dangereux pour l’utilisateur, le patient ou une tierce personne.
- Blessure vasculaire ou tissulaire
- Infection post-opératoire
- Réaction inflammatoire
- Désassemblage des composants
- Usure prématurée / détérioration des instruments due à un mauvais usage
8) MANIPULATION DES INSTRUMENTS
L’établissement de santé est responsable du pré-nettoyage, du nettoyage et de la stérilisation des instruments avant utilisation, conformément aux méthodes validées. Les recommandations suivantes ne se substituent pas aux règles sanitaires en vigueur : normes, guides, notices gouvernementales, textes ministériels, etc. Un procédé de nettoyage réalisé sans respecter les plages de validation peut mener à des risques de toxicité ou nuire à l’état stérile de l’instrument.
D’un point de vue fonctionnel, une inspection doit être réalisée avant utilisation pour vérifier l’absence de bavure ou de débris qui pourraient endommager les tissus ou les équipements de protection du personnel. Rechercher lors de l’inspection tout signe de corrosion ou de contamination qui pourrait provoquer une infection, une réaction inflammatoire, ou des casses d’instrument. De plus, l’intégrité des instruments doit être vérifiée (taille ou prise en main anormale, surface endommagée ou usée, éclats de matériaux, lisibilité du marquage et des mesures et jeu, état des lames de couteaux et ciseaux). Enfin la fonctionnalité (ouverture, fermeture, arrêt) des dispositifs doit être vérifiée plusieurs fois avant l’opération : ils ne doivent pas présenter trop de résistance. Tout dispositif jugé défectueux ou non fonctionnel de quelque manière que ce soit doit être retourné à FIMCO pour maintenance ou échange. Les instructions ci-après doivent être suivies afin de maintenir une efficacité et une sécurité optimales des instruments :- Les substances de nettoyages et éléments chimiques à base de chlore, d’aldéhydes, d’alcool, d’acides ou d’abrasifs susceptibles d’endommager les instruments ne doivent pas être utilisés.
- L’acide phosphorique ne doit pas être utilisé pour la neutralisation des résidus alcalins après le cycle de nettoyage automatisé en machine sur les boites d’instruments et sur les instruments constitués de pièces en polymères (exemple : manches).
- La température de pré-désinfection devrait être < 45°C pour éviter le risque de fixation de résidus.
Il est impératif que les consignes d’utilisation, température, concentration, temps d’action, etc., soient strictement respectées. Sinon, des problèmes peuvent survenir avec les instruments, tels que des changements visuels sur les matériaux (changement de couleur).
Si de l’oxydation se forme sur un instrument, il peut contaminer les autres ; par conséquent les instruments oxydés ne doivent pas être mélangés avec les instruments intacts afin d’éviter les contacts qui pourraient être dangereux pour la stérilisation.
Tout personnel en contact avec des instruments souillés devrait observer une bonne hygiène et utiliser des équipements de protection appropriés (gants, masque, tablier, etc.).
Les dispositifs tranchants ou pointus doivent être manipulés avec la plus grande attention.
a. Graissage et lubrification
Après utilisation et nettoyage, il est parfois nécessaire de lubrifier les pièces articulées ou toute partie mouvante des instruments. Utiliser uniquement une huile de maintenance stérilisable et perméable à la vapeur d’eau. Une huile blanche sans additif, avec une biocompatibilité certifiée et approuvée pour la stérilisation (chaleur humide) est nécessaire. Appliquer la dose d’huile appropriée à la taille de l’instrument directement sur la zone de l’articulation. Répartir l’huile uniformément en ouvrant et fermant plusieurs fois l’instrument. Éliminer l’huile en excès avec un chiffon non pelucheux propre.
b. Contrôle, maintenance et vérification
Après chaque utilisation et nettoyage :- Laisser l’instrument refroidir à température ambiante après nettoyage.
- Vérifier la propreté, la fonctionnalité et les dommages de l’instrument, et isoler les instruments qui sont tordus, déformés, usés, pliés, cassés, fissurés, ou les instruments dont les pièces sont démontées.
- Vérifier la compatibilité entre les instruments associés.
- Retirer immédiatement un instrument abîmé.
c. Conditionnement
- Protéger les instruments avec de fines pointes.
- Placer l’instrument dans son compartiment de stockage ou sur le plateau approprié. Veiller à ce que les lames coupantes soient protégées.
- Conditionner les plateaux en accord avec le procédé de stérilisation (veiller à ce que l’emballage empêche toute nouvelle contamination de l’instrument entre la phase finale de son traitement et sa prochaine utilisation).
- Conditionner les instruments dans des emballages de stérilisation appropriés permettant le maintien de l’état stérile jusqu’à la prochaine utilisation.
- Pour les périodes longues, les micropinces (F250A, F250A5, F251A, F251A5, F251A9, F251B, F251B5, F253A, F253A5, F253A9, F253B, F254A, F255A, F143MI et F144MI) doivent être lubrifiées à la fin du pré-nettoyage (voir partie 9).
9) TRAITEMENT DE PRÉ-NETTOYAGE
Les micropinces (F250A, F250A5, F251A, F251A5, F251A9, F251B, F251B5, F253A, F253A5, F253A9, F253B, F254A, F255A, F143MI et F144MI) doivent être nettoyées avant nettoyage automatique, via la canule fournie avec l’instrument et le produit de nettoyage de l’établissement de santé :- Phase 1 : Insérer la canule dans le trou
- Phase 2 : Injecter le produit de nettoyage
- Phase 3 : Répéter les phases 1 et 2 avec de l’eau contrôlée
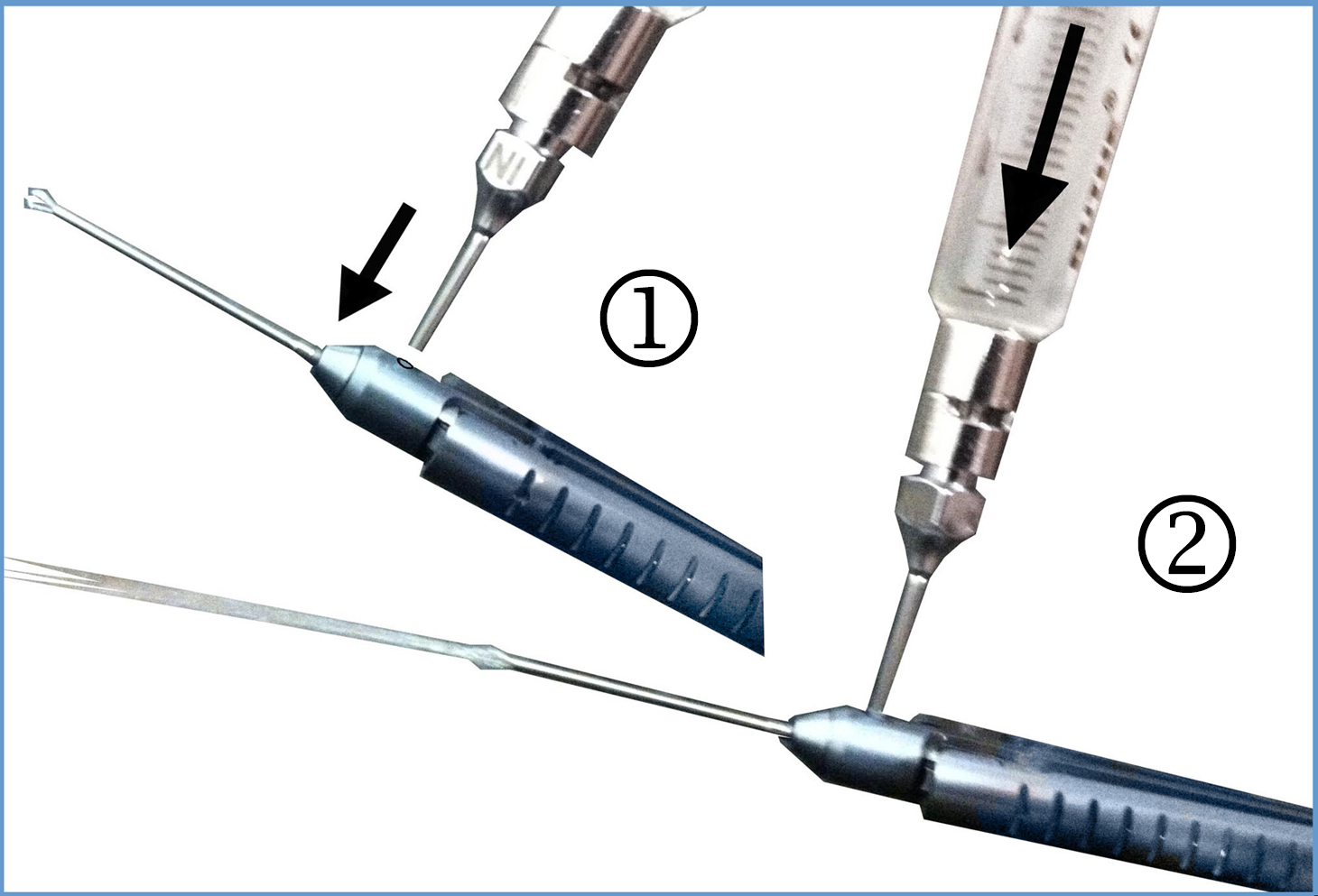
Les résidus séchés peuvent compliquer le procédé de nettoyage et le rendre inefficace ou accélérer la corrosion de l’acier inoxydable. Le procédé de pré-désinfection vise à rendre le nettoyage suivant plus facile. Il est aussi destiné à protéger le personnel lors de la manipulation des instruments et à éviter la contamination de l’environnement.
Tous les dispositifs réutilisables doivent subir un traitement de pré-désinfection immédiat ou être traités immédiatement dans un laveur-désinfecteur après utilisation. Si la pré-désinfection immédiate est impossible, les instruments peuvent être conservés dans de l’eau déminéralisée jusqu’à la pré-désinfection.
- Le traitement de pré-désinfection est réalisé par trempage des instruments, pendant au moins 15 minutes, dans une solution neutre ou alcaline qui ne contient pas d’aldéhyde ou d’éthanol. Utiliser de préférence une solution qui ne fixe par les protéines. Suivre strictement les consignes d’utilisation et s’assurer que les produits sont compatibles avec les instruments.
- Utiliser des produits de nettoyage et de désinfection appropriés. S’il y a un délai entre la pré-désinfection et le lavage, rincer abondamment l’instrument à l’eau courante avant de le nettoyer et de le désinfecter avec un laveur-désinfecteur.
- Si besoin, nettoyer les instruments avec des ultrasons, voir section Nettoyage.
- Retirer tous résidus organiques visibles (sang, os, etc.), une attention spéciale devra être portée aux dispositifs creux ou rainurés.
- L’utilisation de brosses métalliques, d’éponges abrasives ou d’autres articles susceptibles d’endommager les instruments doit être évitée. L’utilisation de brosses à poils souples et de tampons de dimensions adaptées aux dispositifs à traiter est préférable pour nettoyer les pièces de tous les résidus biologiques (sang, os, ...) qui peuvent potentiellement altérer l’action des détergents et des décontaminants. Accorder une attention particulière aux dispositifs canulés.
- L’utilisation d’une action mécanique par des moyens manuel ou par des ultrasons est recommandée (§10)a).
- Les instruments qui peuvent être démontés devraient l’être avant le procédé de pré-désinfection (excepté pour les canules double courant qui devraient rester assemblées tout du long). En outre, les dispositifs dont les composants mobiles ne facilitent pas le démontage devraient être articulés manuellement pendant l’étape de traitement de pré-désinfection afin d’évacuer les résidus supplémentaires.
- Plonger de préférence les instruments dans une solution de nettoyant de type enzymatique et de désinfectant combinés qui ne lie pas les protéines. Eviter l’utilisation de désinfectants contenant des aldéhydes qui ont un effet liant. Respecter les conditions d’utilisation recommandées par le fabricant et s’assurer de la compatibilité du produit avec les instruments.
- Les instruments devraient ensuite être soigneusement rincés dans une eau contrôlée pour éviter les interférences entre solutions de nettoyage. Il est important de se référer aux instructions fournies par le fabricant de ces produits.
- De longues périodes d’attentes pour le traitement sont à éviter – ex : dans la nuit ou les week-ends – à cause du risque de corrosion et de l’efficacité du nettoyage. L’immersion dans de l’eau déminéralisée empêche les résidus de sécher et favorise le nettoyage suivant.
- Dans le cas de longues périodes entre la pré-désinfection et le nettoyage, laver les instruments dans de l’eau contrôlée avant le nettoyage et la désinfection dans un laveur-désinfecteur.
- La stérilisation à la vapeur à 134°C pendant 18 minutes,
- L’immersion dans de l’hydroxyde de sodium à 1N pendant 1 heure à température de la pièce,
- L’immersion dans de l’hypochlorite de sodium 20,000 ppm pendant 1 heure à température de la pièce.
- Le soin et l’entretien sont essentiels pour améliorer la durée de vie et l’efficacité des instruments.
- Ne pas plier ou appliquer de fortes contraintes sur les instruments, car cela peut provoquer une rupture ou une défaillance, entraînant des blessures pour le patient ou l’opérateur.
- N’essayez pas de modifier l’instrument.
- L’utilisateur doit s’assurer que l’équipement est en bon état et fonctionne correctement avant de l’utiliser et, en particulier, qu’il n’y ait aucune trace de corrosion.
- Inspecter visuellement chaque instrument avant de l’utiliser afin de détecter et d’isoler tout instrument usé, déformé, tordu, endommagé, contaminé ou défectueux. Ces instruments doivent être remplacés immédiatement par des instruments neufs (à l’exception des instruments contaminés qui doivent être nettoyés, désinfectés et stérilisés avant d’être utilisés).
- Tous les instruments, s’ils sont utilisés fréquemment, sont sujets à une usure naturelle. Remplacez régulièrement les instruments les plus fréquemment utilisés et les plus fragiles, surtout s’ils ont tendance à se tordre, à se déformer ou à s’user (notamment les sondes et les manipulateurs).
- Si un instrument est cassé pendant l’opération, tous les fragments et débris cassés doivent être retirés du patient.
- Veillez à ce qu’aucune humidité ne subsiste sur la zone de marquage au laser. Si une tache brunâtre se forme, essuyez fortement la tache avec un chiffon doux.
- Pendant l’intervention, les dispositifs peuvent subir diverses forces qui ne peuvent être totalement anticipées. Même avec un retraitement, un entretien et une inspection appropriés, les dispositifs peuvent atteindre la fin de leur durée de vie pendant l’opération. Un remplacement ou une alternative doit être disponible pour le chirurgien.
- Les instruments FIMCO doivent être utilisés uniquement pour les fonctions pour lesquelles ils sont prévus.
- Dans le cas de la référence F807C (myomètre Roth-Rapp), il est obligatoire de réaliser toute traction dans l’axe de l’instrument (axe longitudinal). Sinon l’évaluation de l’élongation du muscle sera erronée.
- Les sondes de Galezowski (F600A, F601A, F602A, F603A, F604A, F605A, F606A, F607A, F608A, F609A, F610A, F610B), et sondes doubles de Bowman (F610C, F611A, F612A, F613A, F614A et F614B), doivent être le plus aligné possible à l’axe du canal lacrymal, de l’insertion au retrait. Sinon, les dispositifs risquent de se briser et de blesser le patient.
ATTENTION : Les plateaux et paniers ne doivent pas être en contact avec des solutions de décontaminations pendant une longue période. Les canules nickelées-chromées et les boîtes en aluminium ne doivent jamais être en contact avec de l’hydroxyde de sodium, sinon elles seront corrodées. Nettoyer les zones sales et les rincer immédiatement.
10) NETTOYAGE
Les instruments doivent être minutieusement nettoyés après le désassemblage et si l’assemblage/ désassemblage est possible. Nous recommandons l’utilisation exclusive de méthodes mécanisées de pré-désinfection et de nettoyage avec un laveur-désinfecteur conforme aux exigences de la série ISO 15883. Se référer aux instructions du fabricant pour l’utilisation du laveur-désinfecteur. Le détergent doit être compatible avec les applications médicales, les matériaux des instruments et ne présenter aucune toxicité résiduelle connue pour le patient. Dans le cas où le processus ne peut pas être réalisé automatiquement, un processus manuel doit être utilisé en reproduisant les conditions décrites dans les recommandations de nettoyage. Le cycle de nettoyage doit inclure un rinçage final avec une eau contrôlée. La durée, le débit d’eau et les volumes de rinçage doivent être suffisants pour réduire autant que possible le niveau des résidus de produits de nettoyage laissés sur la surface du produit. Les instruments doivent être soigneusement séchés pour éviter toute recontamination.
a. Nettoyage aux ultrasons
Cette méthode de nettoyage est particulièrement adaptée aux instruments filetés ou aux instruments présentant des rainures profondes. L’équipement doit être validé par l’utilisateur et utilisé avec des produits adaptés aux matériaux des instruments. Effectuer un nettoyage par ultrasons pendant 10 à 20 minutes pour pré-nettoyer les instruments présentant des résidus séchés ou comme support mécanique efficace avant le nettoyage et la désinfection en laveur-désinfecteur.
b. Nettoyage automatique
Vérifier que le laveur-désinfecteur est conforme (marquage CE), entretenu et qualifié suivant les normes applicables. Utiliser uniquement des produits compatibles avec les instruments, sans aldéhyde, et qui satisfont le Protocole Standard Prion (PSP) si nécessaire. Suivre les instructions pour la concentration, la température et la durée d’action. Utiliser des détergents à pH neutre ou alcalin.
Suivez les procédures de lavage pour assurer une protection adéquate des instruments. Après le nettoyage et la désinfection en laveur-désinfecteur, vérifiez que tous les résidus ont été éliminés. Si nécessaire, répétez le processus de nettoyage par brossage jusqu’à ce que tous les résidus visibles soient éliminés.
Tableau 1 – Protocole de nettoyage automatique recommandé
| Phase | Durée | Température | Type d’eau / de détergent |
|---|---|---|---|
| Pré-Nettoyage | 4 min | Froide (<30°C) | Eau |
| Nettoyage | 10 min | Chauffée, 55°C | Neodisher Septoclean* 10mL/L(1%) |
| Rinçage intermédiaire | 3 min | >30°C et <60°C | Eau chaude adoucie ou déminéralisée |
| Désinfection thermique | 5 min | Chauffée, 90°C | Eau chaude déminéralisée |
| Séchage | 20 min | Air à 99°C | Non applicable (Air) |
*ou produit strictement équivalent
Le cas échéant, sécher l’humidité résiduelle au moyen d’un cycle de séchage complémentaire dans la machine ou de carrés d’essuyage non pelucheux et d’air comprimé sans particule d’eau liée à la condensation.
Note : Dans le cas de patients suspectés ou atteints d’encéphalopathie spongiforme transmissible EST), la procédure de nettoyage en laveur-désinfecteur doit être effectuée après une procédure de décontamination conforme à l’instruction DGS/RI3/2011/449.
Trois procédures existent, aucune n’est une garantie absolue :L’utilisation de l’hypochlorite de sodium ou de l’hydroxyde de sodium n’est pas recommandée car elles provoquent la corrosion des instruments. Aucune des trois méthodes n’est une garantie absolue. En accord avec le guide de l’Organisation Mondiale de la Santé (OMS), la méthode la plus sûre et la moins ambiguë pour éviter une infectivité résiduelle sur les instruments et autres matériels contaminés est de les jeter et de les détruire par incinération.
11) STÉRILISATION
Les instruments doivent être stérilisés avant utilisation. Ils doivent être compatibles avec la stérilisation par vapeur d’eau à une température qui n’excède pas 140°C. En accord avec les instructions gouvernementales sur la non-transmission des agents transmissibles non-conventionnels et les normes en vigueur (notamment l’ISO 17665-1), nous recommandons d’utiliser une stérilisation par vapeur d’eau (conformément aux exigences de la série ISO 17665) avec un cycle validé qui inclus une durée de 18 minutes à 134°C/2bars et suivie par un cycle de séchage sous vide de 30 minutes au moins. L’emballage utilisé doit être marqué CE pour une utilisation comme barrière stérile pour la stérilisation en autoclave. Utiliser du papier absorbant pour l’emballage avant d’utiliser les produits. Le cycle de stérilisation et de séchage doit être validé par l’utilisateur final selon les recommandations du fabricant du stérilisateur.
Les instruments doivent être conditionnés dans un emballage approprié permettant le maintien de l’état stérile. Indiquer sur le sachet la date de stérilisation et la date de péremption conformément aux données du fabricant du sachet.
Tout autre méthode de stérilisation (oxyde d’éthylène ou peroxyde d’oxygène à basse température) n’est pas recommandée et est de la seule responsabilité de l’utilisateur.
Les instruments doivent être préparés de telle façon que toutes les surfaces soient en contact direct avec la vapeur d’eau : les instruments à charnière et les instruments coulissants doivent être légèrement ouverts. Les instruments avec des protections portant la mention "STERILISABLE" doivent être stérilisés avec celles-ci. Les instruments complexes démontables manuellement doivent être démontés, et toutes les pièces doivent être calées dans la boîte de stérilisation. Les établissements de santé doivent valider et qualifier, à l’aide de techniques appropriées, leurs équipements et méthodes utilisés pour la stérilisation par autoclave, conformément aux normes en vigueur pour la stérilisation des dispositifs médicaux par chaleur humide. L’établissement de santé assume la responsabilité finale de la validité de la stérilisation des produits et de leur maintien dans cet état.
Les recommandations de stérilisation sont données à titre d’information uniquement.
L’utilisateur/l’opérateur doit se conformer aux lois et règlements du pays dans lequel il est établi. En aucun cas, le fabricant ne peut être tenu responsable de la stérilité des dispositifs stérilisés au sein de l’établissement de santé.
12) RÉUTILISATION DES INSTRUMENTS
Les instruments sont destinés à être réutilisés. Le nombre de réutilisations dépend de l’intégrité de chaque instrument. Il n’y a pas de limite théorique à leur réutilisation tant qu’ils respectent les performances revendiquées et à condition qu’ils ne présentent pas de signe d’usure, de distorsion, de dommage ou de perte de performance.
Avant d’être réutilisés, les dispositifs doivent être pré-désinfectés, nettoyés et stérilisés (comme décrit dans les sections précédentes).
13) STOCKAGE, MANIPULATION ET TRANSPORT
Les instruments chirurgicaux doivent être manipulés avec soin et doivent être stockés dans une salle propre dans des conditions normales d’humidité. Les instruments doivent être protégés des rayons UV et de tout environnement corrosif. Quand des instruments stérilisés doivent être transportés sur le site d’utilisation (bloc opératoire), le caractère stérile doit être maintenu. Utiliser un conditionnement stérile pour maintenir l’état stérile des instruments.
Rester vigilant à propos des risques de chutes et/ou de blessures.
Les instruments usés doivent être transportés au service d’approvisionnement dans un conditionnement fermé ou couvert pour éviter une contamination non-nécessaire. Une chute peut entraîner la rupture ou l’endommagement de l’instrument et/ou des blessures pour l’opérateur. Utiliser des plateaux ou des conteneurs rigides.
14) ÉLIMINATION ET INSTRUMENTS NON-FONCTIONNELS
La fin de vie de chaque dispositif est déterminée lorsque les caractéristiques ou les performances du dispositif indiquent que la santé ou la sécurité du patient ou de l’utilisateur peuvent être compromises. La durée de vie du dispositif dépend de nombreux facteurs, y compris, mais sans s’y limiter, la méthode et la durée d’utilisation et le niveau de retraitement. Par conséquent, FIMCO ne définit pas de nombre maximum d’utilisations. Une inspection minutieuse et des tests fonctionnels doivent être effectués. Examinez les arêtes de coupe, les becs, les pointes, les axes, les manches et les caractéristiques de l’extrémité de travail, selon le cas, pour détecter tout émoussage, écaillage, déformation, fissure ou autre indication de dégradation du matériau ou de compromission de l’intégrité structurelle.
Le marquage laser doit rester lisible. Si le dispositif présente l’un de ces signes d’usure ou d’autres indications de dysfonctionnement, il est recommandé d’arrêter l’utilisation et de remplacer le dispositif. Actionner les pièces mobiles et assembler les dispositifs pour vérifier qu’ils ne sont pas coincés ou obstrués. Si les pièces mobiles ou assemblées présentent une fonctionnalité limitée, remplacer le(s) dispositif(s).
FIMCO assure des prestations de réparation (remise à neuf) pour ses instruments, et peut évaluer l’état d’un instrument. Tout dispositif non-fonctionnel ou à réparer doit être renvoyé à FIMCO à l’état-stérile et avec une preuve de stérilisation, car FIMCO assure l’élimination sûre de ses dispositifs. En cas d’envoi d’un instrument non-fonctionnel sans preuve de stérilisation, l’instrument sera renvoyé à l’établissement de santé.
15) DANGERS ET PRÉCAUTIONS
Le fabricant recommande que tout le personnel responsable de la manipulation et de l’utilisation des dispositifs lise et comprenne ces informations avant utilisation. L’utilisation de l’instrumentation chirurgicale nécessite des connaissances en anatomie, biomécanique et chirurgie ophtalmologique.
L'instrumentation chirurgicale ne doit être utilisée que par un chirurgien qualifié opérant conformément aux informations actuelles sur l'état des progrès scientifiques et l'état de l'art de la chirurgie ophtalmologique.
Note : Les instructions fournies dans cette notice ont été validées par FIMCO pour préparer les instruments chirurgicaux réutilisables de FIMCO en vue de leur réutilisation. Il est de la responsabilité de l’utilisateur/du responsable de traitement de s’assurer que le traitement, tel qu’il est effectivement réalisé en utilisant l’équipement, le matériel et le personnel de traitement, permet d’obtenir le résultat souhaité. Cela nécessite une vérification et/ou une validation et un contrôle de routine du processus.
Il est de la responsabilité du chirurgien de fournir au patient toutes les informations nécessaires avant l’opération, y compris les effets indésirables liés à l’opération, aux implants et aux instruments.
FIMCO décline toute responsabilité en cas d’incidents liés à l’intervention sur l’instrument par une personne non habilitée. La garantie ne s’applique pas en cas de démontage, modification ou intervention effectués sur l’instrument en dehors de FIMCO.
FIMCO ne peut être tenu responsable de tout préjudice direct ou indirect subi par le client en cas d’utilisation, d’entretien, de nettoyage ou de stérilisation inappropriés du dispositif médical.
16) INCIDENT GRAVE
“Incident grave” signifie tout incident qui, directement ou indirectement, a conduit, aurait pu conduire ou pourrait conduire à l’une des situations suivantes : le décès d’un patient, d’un usager ou d’une autre personne ; la détérioration grave temporaire ou permanente de l’état de santé d’un patient, d’un usager ou d’une autre personne ; une menace grave pour la santé publique.
Tout incident grave qui s’est produit en relation avec les instruments de FIMCO doit être rapporté à FIMCO et à l’autorité compétente de l’État Membre dans lequel l’utilisateur et/ou le patient est établi.

Version i - 20/06/2022
